Los calores o
entalpías de sublimación (DsubHº) de compuestos
sólidos o de vaporización (DvapHº) de
compuestos líquidos, son magnitudes relacionadas con la energía de las interacciones
intermoleculares en la fase condensada (sólida o líquida). Su valor depende de
la estructura, tamaño y polaridad de la molécula.
En el siguiente
gráfico ilustramos el concepto de la entalpía de transición de fase condensada
a fase gas.

Los valores de
estas entalpías se usan fundamentalmente para convertir la entalpía de
formación de un compuesto del estado condensado (sólido o líquido) al estado
gaseoso
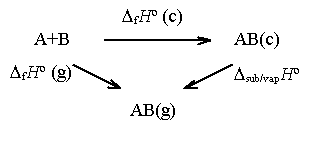
DfHº(g) = DfHº(cd) + Dvap/subHº(g)
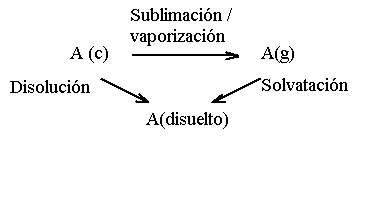
Permiten además,
el cálculo de entalpías de solvatación al combinarlas con entalpías de disolución.